Ons klinische programma met filgotinib voor de ziekte van Crohn
Onze FITZROY Fase 2 studie (174 patiënten) betrof een evaluatie van filgotinib eenmaal daags vergeleken met placebo bij patiënten met matige tot ernstige ziekte van Crohn en verzwering van het darmslijmvlies. Ingeschreven patiënten waren ofwel naïef voor, of vertoonden geen reactie op, anti-TNF-middelen. FITZROY was de eerste studie in de ziekte van Crohn waarin bij aanvang endoscopische bevestiging van laesies en tevens een placebocontrole bij de endoscopie vereist was. De studie bestond uit twee delen, elk met een duur van 10 weken: in het eerste deel werden de veiligheid en werkzaamheid van filgotinib 200 mg eenmaal daags onderzocht, vergeleken met placebo; het tweede deel betrof een verkennend observatieonderzoek van de gedurende 20 weken voortgezette behandeling. De FITZROY-studie heeft het primaire eindpunt van klinische remissie na 10 weken bereikt: het percentage patiënten bij wie de CDAI-score (Crohn’s Disease Activity Index) lager was dan 150 was statistisch gezien significant hoger bij de met filgotinib behandelde patiënten (47%) dan bij patiënten die een placebo kregen (23%). Het percentage patiënten bij wie sprake was van een klinische respons van 100 punten (60%) was ook significant vergeleken met de placebogroep (41%). Ook verbetering in de kwaliteit van leven, histopathologie, endoscopisch onderzoek en biomarkers van ontstekingsactiviteit werden in week 10 waargenomen. De algehele gemiddelde verandering van de histopathologiescores in week 10 voor met filgotinib behandelde patiënten (-3,5) t.o.v. placebo (-0,6) vertoonde een significant verschil, waarmee de klinische respons in de weefsels van patiënten werd bevestigd. Er waren meer met filgotinib behandelde patiënten bij wie sprake was van >50% verbetering van de in SES-CD-scores (endoscopie) vergeleken met placebo in week 10:
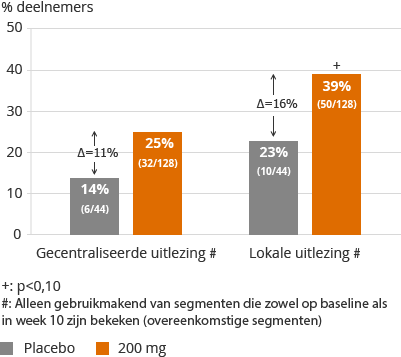
Vermeire et al., The Lancet, 2016
De klinische respons bleef van week 10 t/m week 20 gehandhaafd. Patiënten in de placebogroep bij wie in de eerste tien weken geen respons optrad, kregen in de tweede tien weken 100 mg filgotinib en vertoonden verbetering in klinische remissie gedurende het tweede deel van de studie.
Over het algemeen blijkt uit de FITZROY studie na 20 weken behandeling, dat filgotinib een gunstig veiligheidsprofiel laat zien, overeenkomstig de DARWIN-studies in reumatoïde artritis. In FITZROY werd tevens een toename van hemoglobine waargenomen, zonder verschil tussen filgotinib en placebo. Er zijn geen opvallende veranderingen in neutrofielen of leverfunctietesten ten opzichte van de basiswaarden waargenomen.
Gilead is in november 2016 een Fase 3-studie (DIVERSITY) gestart met filgotinib in de ziekte van Crohn. De DIVERSITY Fase 3 studie onderzoekt de werkzaamheid en veiligheid van eenmaal daagse toediening van 100 mg en 200 mg filgotinib vergeleken met placebo bij patiënten met matige tot ernstige ziekte van Crohn, met inbegrip van patiënten bij wie eerdere antilichaamtherapie niet heeft gewerkt. Gilead zal circa 1.300 patiënten werven in de VS, Europa, Latijns-Amerika, Canada en Azië/Pacific. Mannen en vrouwen in de DIVERSITY studie worden gerandomiseerd voor placebo, 100 mg of 200 mg filgotinib. In de VS kunnen mannen 200 mg krijgen als bij hen na ten minste één anti-TNF en vedolizumab – een monoklonaal anti-integrine antilichaam op de markt gebracht door Takeda – geen respons optrad.
In maart 2017 is Gilead met twee nieuwe Fase 2 studies met filgotinib in de ziekte van Crohn gestart, in de dunne darm en bij fistelvorming.
